Metastasiertes, hormonsensitives Adenokarzinom
der Prostata (mHSPC)
Studie PSMAddition
To determine whether the therapy with 177Lu-PSMA-617 in combination with ARDT and ADT improves the radiographic progression free survival compared to the standard of care, ARDT and ADT alone, in metastatic hormone sensitive prostate cancer (mHSPC) participants that were previously minimally treated.
Welche Patientengruppe wird in die Studie eingeschlossen?
Patienten mit einem metastasierten, hormonsensitiven Adenokarzinom der Prostata (mHSPC),
die noch keine Hormonentzugstherapie oder kürzlich (< 45 Tage) eine Hormonentzugstherapie
erhalten haben. Zusätzlich müssen alle Metastasen im PSMA-PET/CT eine PSMA-Aufnahme
zeigen. Eine vorherige Therapie mit einem Androgentarget oder eine Chemotherapie ist nicht
erlaubt.
Welche Vortherapien sind erlaubt?
- Radikale Prostatektomie
- Strahlentherapie der Prostata
- Max. 45 Tage Vorbehandlung mit LHRH-Agonisten oder LHRH-Antagonisten als
Hormonentzugstherapie.
- Max. 45 Tage Vorbehandlung mit Abirateron, Apalutamid, Enzalutamid oder Darolutamid
als Androgentarget-Therapie
Welche Vortherapien sind nicht erlaubt?
- Radionuklide wie z.B. Radium-223 Therapie oder PSMA-Lutetium Therapie
- Taxanhaltige Chemotherapie, Immuntherapie oder PARP-Inhibitoren
Gibt es Ausschlusskriterien für die Studie?
- Zweittumor in den letzten 3 Jahren
- Symptomatische Hirnmetastasierung
- Kardiale Erkrankungen z.B. III AV-Block, QT-Syndrom, u.a.
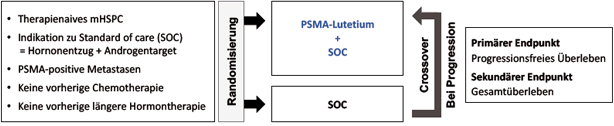
Wie funktioniert die Phase-III Studie?
Patienten mit einem mHSPC werden nach dem Zufallsprinzip in zwei Gruppen aufgeteilt. Die
Standardgruppe erhält eine Hormonentzugstherapie mit einem Androgentarget. Die
Studiengruppe erhält zusätzlich eine Radioliganden-Therapie mit PSMA-Lutetium sowie eine
Hormonentzugstherapie mit einem Androgentarget. Die Studie ist nicht verblindet, sodass
sowohl der Patient als auch der Arzt wissen, welche Therapie verabreicht wird.
Was für eine neue Tumortherapie wird untersucht?
Der Radioligand PSMA-Lutetium wirkt über eine radioaktive Strahlung. Er bindet gezielt an das
Eiweiß PSMA auf der Oberfläche von Prostatakrebszellen, welche die Therapiesubstanz in die
Tumorzelle aufnehmen. Durch die lokale Bestrahlung kommt es dann zur Zerstörung der
Tumorzellen. Eine Kombination aus Hormontherapie und Strahlentherapie verstärkt die DNASchäden
in der Tumorzelle und bewirkt eine effektivere Zerstörung der Tumorzellen.
Wie ist die Studie aufgebaut?