Metastasiertes kastrationsresistenes Prostatakarzinom
mCRPC
Study of Nivolumab or Placebo in Combination with Docetaxel, in Men with Metastatic Castration-resistant Prostate Cancer (CheckMate 7DX: CHECKpoint pathway and nivoluMAB clinical Trial Evaluation 7DX)
Welche Patientengruppe wird in die Studie eingeschlossen?
Patienten mit einem metastasierten kastrationsresistenten Prostatakarzinom (mCRPC), die unter einer Androgentarget-Therapie im mCRPC-Stadium ein weiteres Tumorwachstum zeigen. Es müssen entweder mind. eine Knochenmetastase und/oder eine messbare Weichteilmetastase vorhanden sein.
Welche Vortherapien sind erlaubt?
- Docetaxel im mHSPC-Stadium
- Maximal 2 Androgentarget-Therapien, davon eine im mHSPC Stadium
- Radionuklidtherapie (Radium223, PSMA-Lutetium)
Welche Vortherapien sind nicht erlaubt?
- Immuntherapien
- Hochdosiertes Kortison
Gibt es Ausschlusskriterien für die Studie?
- Zweittumor in den letzten 2 Jahren
- Demenz, aktive Hirnmetastasen
- Höhergradige periphere Polyneuropathie
- Herzinsuffizienz, instabile AP, kardiale Arrhythmien
- Superscan in der Skelettszintigraphie
Wie funktioniert die Phase-III Studie?
Patienten mit einem mCRPC werden in zwei verschiedene Therapiearme per Zufallsprinzip randomisiert. Dabei ist die Studie verblindet: Weder Patient noch Arzt wissen, ob eine Immuntherapie oder eine Placebo-Infusion intravenös verabreicht wird.
Was für eine neue Tumortherapie wird untersucht?
Klassische Chemotherapie mit Docetaxel plus Immuntherapie mit Nivolumab als ambulante Kurzinfusion im 3-Wochenintervall. Neu ist die Immuntherapie mit dem Checkpoint-Inhibitor Nivolumab, die zu einer Reaktivierung des eigenen Immunsystems gegen die Tumorzellen führt.
Wie ist die Studie aufgebaut?
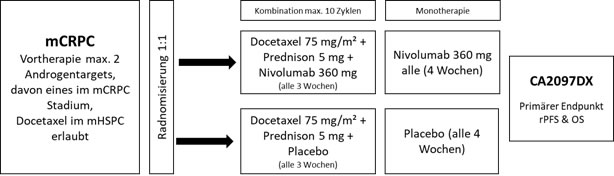
Wo finde ich ausführliche Informationen:
www.clinicaltrials.gov NCT04100018
