Metastasiertes hormonsensitives Prostatakarzinom
mHSPC
Study of Niraparib in Combination with Abiraterone Acetate and Prednisone Versus Abiraterone Acetate and Prednisone for the Treatment of Participants with Deleterious Germline or Somatic Homologous Recombination Repair (HRR) Gene-Mutated Metastatic Castration-Sensitive Prostate Cancer (mCSPC) (AMPLITUDE)
Welche Patientengruppe wird in die Studie eingeschlossen?
Patienten mit einem metastasierten hormonsensitiven Prostatakarzinom (mHSPC) mit mindestens einer Knochenmetastase. Zusätzlich wird eine spezielle Änderung der Erbinformation (HRR Keimbahn- oder somatische Mutation) im Prostatatumorgewebe oder im Blut von Prostatakrebspatienten nachgewiesen.
Welche Vortherapien sind erlaubt?
- Hormonentzugstherapie für mindestens 2 Wochen und maximal 6 Monate
- Docetaxel-Chemo mit max. 6 Zyklen, nach Abschluss kein Tumorwachstum
Welche Vortherapien sind nicht erlaubt?
- PARP-Inhibitor, Ketoconazol, Enzalutamid, Apalutamid oder Darolutamid
- Checkpoint-Inhibitoren
Gibt es Ausschlusskriterien für die Studie?
- Zweittumor in den letzten 2 Jahren
Wie funktioniert die Phase-III Studie?
In dieser Studie erhält jeder Patient die Hormonentzugstherapie und das Antiandrogen Abirateron plus Prednison. Die zu prüfende Substanz Niraparib wird in zwei verschiedene Therapiearme per Zufallsprinzip randomisiert. Dabei ist die Studie verblindet: Weder der Patient noch der Arzt wissen, ob die Kombination aus Abirateron/Prednison plus Niraparib oder nur Abirateron/Perdnison plus Placebo verabreicht wird.
Was für eine neue Tumortherapie wird untersucht?
Das klassische Antiandrogen Abirateron plus Prednison führt zu einer effektiven Unterdrückung der Tumoraktivität von Prostatakrebszellen. Niraparib ist ein PARP-Inhibitor. Es verhindert die Reparatur von fehlerhaften Genen in den Prostatakrebs-zellen und führt schließlich zum Absterben der Tumorzellen. Prostatakrebszellen mit zusätzlich Nachweis einer HRR-Mutation reagieren besonders empfindlich auf Niraparib und führen zum raschen Absterben der Krebszellen.
Wie ist die Studie aufgebaut?
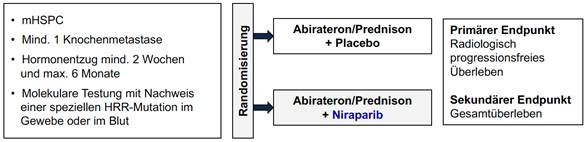
Wo finde ich ausführliche Informationen:
www.clinicaltrials.gov NCT04497844
